Unatoč sličnom imenu, eteri i esteri su dvije potpuno različite klase spojeva. Dobivaju se na različite načine. Oni imaju različita kemijska svojstva. Razlikuju se po strukturnoj formuli. Sve u svemu, postoje samo neka fizička svojstva njihovih najpoznatijih predstavnika.
Fizikalna svojstva estera i estera
Eteri su slabo topljivi u vodi, tekućinama s niskim vrelištem, lako zapaljivi. Na sobnoj temperaturi eteri su ugodno mirisne bezbojne tekućine. 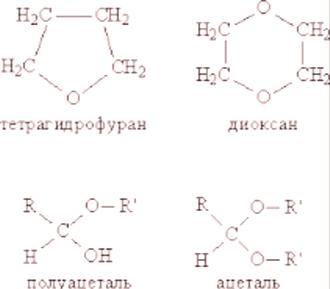
Esteri niske molekularne mase - lako isparavajuće bezbojne tekućine, dobro mirišu, često voće ili cvijeće. S povećanjem ugljikovog lanca ostataka acilne skupine i alkohola, njihova se svojstva razlikuju. Takvi eteri su krute tvari. Njihova točka taljenja ovisi o duljini ugljikovih radikala i strukturi molekule.
Struktura etera i estera
Oba spoja imaju etersku vezu (-O-), ali u estrima ona je dio složenije funkcionalne skupine (-COO), u kojoj je prvi atom kisika vezan za atom ugljika jednostrukom vezom (-O-), i drugi dvostruki (= O).
Shematski se može prikazati kako slijedi:
- Eter: R - O - R1
- Ester: R - COO - R1
Ovisno o radikalima u R i R1, eteri se dijele na:
- Simetrični esteri - oni u kojima su alkilni radikali identični, na primjer, dipropil eter, dietil eter, dibutil eter i slično.
- Asimetrični ili miješani esteri s različitim radikalima, na primjer, etil propil eter, metilfenil eter, butil izopropil, itd.
Esteri se dijele na:
- Esteri alkohola i mineralne kiseline: sulfat (-SO3H), nitrat (-NO2), itd.
- Esteri alkohola i karboksilne kiseline, na primjer C2H5CO-, C5H9CO-, CH3CO-, itd.
Razmotriti kemijska svojstva estera. Eteri imaju nisku reaktivnost, zbog čega se često koriste kao otapala. Reagiraju samo u ekstremnim uvjetima ili s vrlo reaktivnim spojevima. Za razliku od estera, esteri su reaktivniji. Oni lako ulaze u reakcije hidrolize, saponifikacije, itd.
Eteri
Reakcija etera s vodikovim halogenidima:
Većina etera može se razgraditi pri izlaganju bromovodičnoj kiselini (HBr) kako bi se formirali alkil bromidi ili u interakciji s jodovodičnom kiselinom (HI) kako bi se proizveli alkil jodidi.
CH3-0-CH3 + HI = CH3-OH + CH3I
CH3-OH + HI = CH3I + H2O
Stvaranje oksonijevih spojeva:
Sumporna, jodna i druge jake kiseline pri međudjelovanju s eterima iz oksonijevih spojeva - produkti spojaviši poredak.
CH3-0-CH3 + HCl = (CH3) 20O HCl
Interakcija etera s metalnim natrijem:
Kada se zagrijavaju s osnovnim metalima, kao što je metalni natrij, eteri se dijele na alkoholate i alkil natrij.
SN3 - O - SN3 + 2Na = SN3 - NAa + SN3 - Na
Auto-oksidacija etera:
U prisutnosti kisika, eteri polako auto-oksidiraju u obliku hidroperoksida idalkil peroksida. Auto-oksidacija je spontana oksidacija spoja u zraku.
C2H5 - O - C2H5 + O2 = CH3 - CH (UN) - O - C2H5
Esteri
Hidroliza estera:
U kiselom okolišu, ester hidrolizira u odgovarajuću kiselinu i alkohol.
CH3 - COO - C2H5 = CH3 - COOH + H2O
Saponifikacija estera:
Na povišenim temperaturama, esteri reagiraju s vodenim otopinama jakih baza, kao što su natrijev ili kalijev hidroksid, da se formiraju soli karboksilnih kiselina. Soli ugljičnih kiselina nazivaju se sapunima. Nusproizvod reakcije saponifikacije je alkohol.
CH3 - COO - C2H5 + NaOH = CH3 - COONa + C2H5 - OH
Re-esterifikacijske (izmjene) reakcije:
Esteri ulaze u reakcije razmjene pod djelovanjem alkohola (alkoholize), kiselina (acidoliza) ili dvostruke izmjene, uz interakciju dvaju estera.SN3 - SOO - S2N5 + S3N7 - ON = SN3 - SOO - S3N7 + S2N5 - OH
CH3-COO-C2H5 + C3H7-COOH = C3H7-COO-C2H5 + CH3-COOH
SN3 - SOO - S2N5 + S3N7 - SOO - SN3 = SN3 - SOO - SN3 + S3N7 - SOO - S2N5
Reakcije koje reagiraju s amonijakom:
Esterimože djelovati s amonijakom (NH3) s nastankom amida i alkohola. Po istom principu reagiraju s aminima.
SN3 - SOO - S2N5 + NN3 = SN3 - SO - NHN + S2N5 - OH
Reakcije redukcije estera:
Esteri se mogu reducirati vodikom (H2) u prisutnosti bakrenog kromita (Cu (CrO2) 2).
CH3-COO-C2H5 + 2H2 = CH3-CH2-OH + C2H5-OH







