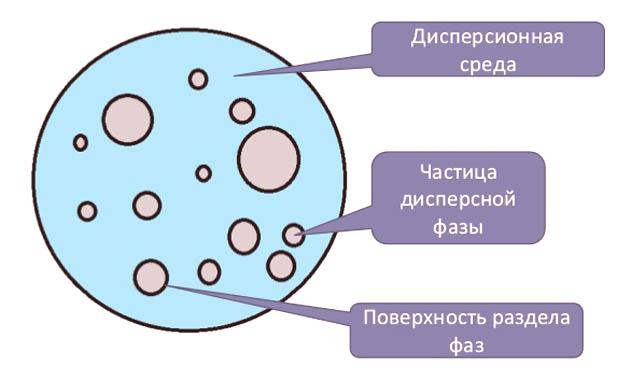
Sastav disperznog sustava
Svojstva i uporaba koloidnih otopina
U širem smislu, u biti, koloidi susvi prirodni organizmi i ekološke biljke , od kojih većinu uzimamo s hranom u koloidnom stanju. Lijekovi, neke boje, pa čak i građevinski materijali (vezni materijali za cement i beton, boje i keramika, zapaljivi materijali, umjetna vlakna, plastika) također se odnose na koloide.
Kinetička svojstva heterogenih disperznih sustava. Kretanje je posljedica razlike u veličini čestica. Tanka suspenzija sposobna za Brownov slučajni pokret. Na primjer, masti dodane u vodu ili mlijeko razrijeđeno vodom. Kretanje čestica koloidne otopine je termodinamički energetski intenzivno.

OstaloKinetičko svojstvo otopina jedifuzija : proces kretanja čestica zbog razlika u njihovim koncentracijama. Ali čvrste grube čestice ne sudjeluju u kaotičnom kretanju, ali glavni razlog njihovog kretanja je razdvajanje gustoće faza u disperziranom mediju. Prema tome, ako je gustoća veća, onda se čestice postupno talože pod djelovanjem gravitacije - procesom taloženja. Vrlo čest proces koji se koristi u molekularnoj kemiji proteina, molekula nukleinskih kiselina, pa čak i bakterija. Osmotski tlak koloida je vrlo mali, budući da koloid ima veliku masu.

Optička svojstva otopine posljedica su sposobnostiraspršiti svjetlo , odnosno prisutnost fenomena opalescencije (zbog optičke nehomogenosti). Primijećeno je, ako prođete snop svjetlosti kroz kivetu, stavljajući leću ispred sebe, a zatim sa strane možete vidjeti učinak (Tyndall konus). To je posljedica ovisnosti veličine čestica otopine i duljine svjetlosnog snopa.
Disperzija se promatra ako je valna duljina veća od veličine čestica u p-re. Ako čestice imaju istu veličinu kao valna duljina, onda ih snop zaokružuje ravno i rasipa, tj. Uočava se fenomen difrakcije. Zbog spektra raspršenja moguće je točno odrediti je li otopina istinska (ionska, molekularna ili koloidna otopina).
Prava rješenja i njihova svojstva
Prava rješenja su transparentne, homogene otopine s krutom disperznom fazom, veličine čestica manjih od jednog nanometra, dakle granicaodvajanje faza u otopini nestaje. Prava otopina se dijeli na ionske, ako se dispergirana faza sastoji od hidratiranih iona (otopina natrijevog klorida ili molekularne (otopine glukoze). Voda igra neizostavan dio života, jer se u njoj otapaju svi ioni tijela, zahvaljujući tome nastaju svi metabolički procesi između stanica.

Razlike između koloida i istinitih rješenja
Prvo, istinska rješenja su transparentna i homogena, a čestice u disperznoj fazi manje su od nanometara. Ne karakterizira ihdifrakcija ili opalescencija , ne postoji Tyndalov konus, tj. Čestice su tako male da nisu ni vidljive u ultramikroskopu. Kada se filtriraju, koloidne otopine ne prolaze kroz papirne filtre, a pravi filtri se lako filtriraju, što pokazuje razlike između veličine čestica disperzne faze. Prava otopina prolazi kroz stanične membrane. Termodinamički, a ne stabilan, slojevit, što je tipično za koloidna rješenja, i istinito - ne stratificiraju se.
Prava rješenja mogu nastati spontano, bez troška dodatne energije i koloidne otopine, naprotiv, energetska bilanca za njih nije stabilna. Transformacijske sile između faze i medija za prave otopine su prilično velike, pa im nije potreban stabilizator. Mehanička svojstva otopina međusobno se razlikuju. Točne otopine su trajnije, budući da je disperzna faza nepokretna, tvori strukturu unutar koje je medij zatvoren (na primjer, koštano tkivo).Koloidna otopina je slobodno dispergirana, ima fluidnost, stoga je koncentracija faze i medija ravnomjerno raspoređena (prašina, dim ili magla).